Las proteínas ¿qué son?
Hola de nuevo, y bienvenidos a un nuevo post, donde vamos a hablar acerca de las proteínas.
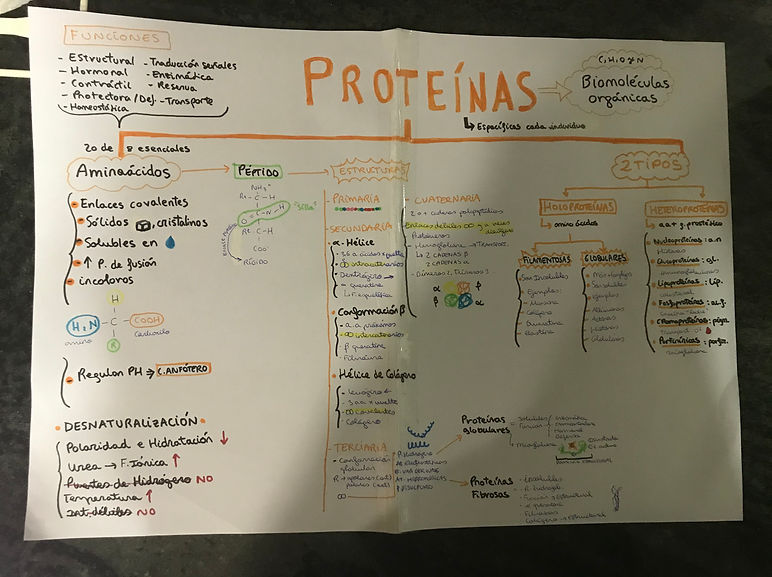
Comenzaré diciendo que son moléculas orgánicas compuestas prinicipalmente por C,H, O y N. Presentan un grupo carboxilo (-COOH), uno amino (-NH2), y una cadena lateral.
Son además, sólidos, solubles en agua, cristalizables, poseen un elevado punto de fusión y actividad óptica.
Dependiendo de su polaridad pueden ser: Hidrófobos, Hidrofílicos o Ácidos básicos.
Según su polaridad pueden ser Hidrófobos, Hidrofílicos, Ácidos o Básicos. Poseen un carácter anfótero, es decir, que pueden comportarse como amortiguador, ósea, como ácido o base para regular el PH.
Cabe destacar que existen 20 aminoácidos proteicos, de los cuales 8 son esenciales y que es necesario como mínimo 2 aminoácidos para formar una proteína.
En cuanto a la clasificación de las proteínas, pueden ser divididas en:
-
Holoproteínas: formadas sólo por aminoácidos. Se diferencian en filamentosas como la miosina y globulares como las albúminas.
-
Heteroproteínas: formadas por aminoácidos y un grupo prostético, dependiendo de éste se clasificarán en nucleoproteínas, cromoproteínas, glucoproteínas, lipoproteínas y fosfoproteínas.
Por otro lado, los enlaces que se forman entre 2 aminoácidos se denominan enlaces peptídicos, los cuáles tienen carácter doble y son cortos. Dependiendo del número de aminoácidos, las cadenas pueden formar:
-Dipéptidos: 2 amino ácidos
-Tripéptidos: 3 aa
-Oligopéptidos: menos de 10 aa
-Polipéptidos: más de 10 aa
Las proteínas forman una estructura tridimensional definida que se puede diferenciar entre cuatro tipos, tenemos:
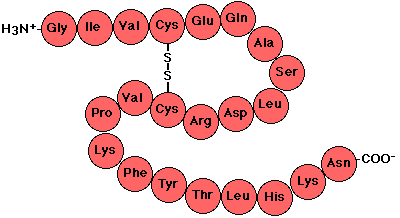
-ESTRUCTURA PRIMARIA-
Es la secuencia lineal de aminoácidos que componen
la proteína y el orden en que se disponen.
Presente en todas las proteínas.
Su disposición en zig zag.
-ESTRUCTURA SECUNDARIA-
Es un nivel más bajo que el primario.
Capacidad de giro gracias a enlaces no peptídicos.
Pueden adoptar 3 formas:
-α-Hélice: La estructura se enrolla en espiral.
Se establecen enlaces intracatenarios.
-β o Lámina Plegada: La estructura sigue siendo de
zig zag
y los enlaces son peptídicos e intercatenarios.
No hay enlaces de Hidrógeno.
-Hélice de colágeno: Estructura rígida que se enrolla
de forma levógira. Los enlaces son por puentes
de hidrógeno.
-ESTRUCTURA TERCIARIA-
La estructura secundaria plegada sobre si misma. Los radicales polares se disponen hacia afuera y los apolares hacia dentro. Los enlaces pueden ser por:
-Enlaces de Hidrógeno
-Interacciones iónicas
-Atracciones hidrofóbicas
-Fuerzas de Van der Waals
-Puentes disulfuro
Dentro de esta estructura
se diferencian dos tipos
dependiendo
de las funciones y características.
Pueden ser:
GLOBULARES: Muy compactas, dan lugar a una estructura prácticamente esférica. Solubles en agua y las funciones que desempeñan son: enzimática, transportadora, defensa y hormonal.
FIBROSAS o FILAMENTOSAS: Forman moléculas alargadas, insolubles en agua y predominan los radicales hidrófobos. Su función principal es estructural.
-ESTRUCTURA CUATERNARIA-
Proteínas formadas por dos o más cadenas cadenas polipéptidicas con estructura terciaria. Se unen mediante enlaces débiles y en ocasiones mediante puentes disulfuro. Cada una de estas cadenas recibe el nombre de protómero. Y según el número de protómeros que se asocian se denominan:
-DÍMEROS: Insulina
-TRÍMEROS: Colágeno
-TETRÁMEROS: Hemoglobina
Finalmente, las proteínas tienen diferentes funciones, que podéis encontrar en el siguiente esquema junto con más información.
ACTIVIDADES
a) Enumerar los cuatro niveles de estructura de las proteínas.
Los niveles de estructura de las proteínas son la estructura primaria, la secundaria en la que podemos distinguir la α-hélice, conformación β o lámina plegada y hélice de colágeno; la terciaria donde encontramos las proteínas globulares y las fibrilares o filamentosas, y la cuaternaria.
b) Indicar qué tipos de enlaces intervienen en la estabilización de cada uno de estos niveles estructurales.
En la estructura primaria se establecen enlaces peptídicos, que son unos enlaces rígidos y muy estables, por lo que se dice que tienen carácter de doble enlace. Por otro lado, en la secundaria intervienen los enlaces covalentes y los puentes de hidrógenos, que en el caso de la α-hélice son intracatenarios y en la conformación β intercatenarios. En cuanto a la estructura terciaria, las uniones pueden ser enlaces de hidrógeno entre grupos peptídicos, atracciones electrostáticas entre grupos con carga opuesta, atracciones hidrofóbicas, fuerzas de Van der Waals o puentes disulfuro entre grupos tiol (-SH) de dos cisteínas, que es un enlace fuerte. Por último, en la estructura cuaternaria los enlaces más comunes son los débiles (no covalentes) o, en ocasiones, enlaces covalentes del tipo disulfuro.
c) Especificar la estructura que caracteriza a las α-queratinas.
La estructura característica de las α-queratinas es la α-hélice de la estructura secundaria. Además, presentan monómeros de cisteína en sus cadenas de aminoácidos, los cuales forman puentes disulfuro.
d) Describir dos propiedades generales de las proteínas.
Especificidad: Las proteínas de los seres vivos son características de cada especie, pero aún así varían dentro de una especie debido al orden de los aminoácidos. Las proteínas que cumplen una misma función en distintos seres vivos, pero no son idénticas se denominan homólogas.
Esta especificidad es importante, ya que si se introduce una proteína de un cuerpo en otro, éste puede reconocerla como un cuerpo extraño y reaccionar contra ella (como ocurre en los rechazos de trasplantes de órganos)
Capacidad amortiguadora: Debido al comportamiento anfótero pueden comportarse como ácidos o como bases, liberando o retirando protones del medio. Así amortiguan las variaciones de pH del medio en el que se encuentran.
e) Describir dos funciones de las proteínas. Indica un ejemplo.
Función de reserva: Almacenan aminoácidos en la ovoalbúmina de la clara del huevo o la caseína de la leche etc.
Función estructural: Las proteínas (sobretodo filamentosas) forman la mayoría de estructuras celulares y orgánicas. Por ejemplo, las glucoproteínas forman parte de la membrana plasmática, la actina y tubulina forman cilios, flagelos, citoesqueleto etc. También tienen esta función las histonas y protaminas, el colágeno, la elastina, queratina etc.
f) Defina el proceso de desnaturalización. ¿Qué tipo de enlaces no se ven afectados?
La desnaturalización consiste en la pérdida de la estructura cuaternaria, terciaria o incluso secundaria de las proteínas. Puede ocurrir debido a cambios de temperatura, pH, concentración de sales o agitación. Al perderse esta estructura se rompen muchos enlaces (pero no los peptídicos)
Cuando una proteína se desnaturaliza precipita, ya que adquiere un aspecto filamentoso (los radicales no se encuentran rodeados de agua)
Se puede dar la renaturalización de las proteínas si las condiciones vuelven a ser óptimas, ya que los enlaces peptídicos no se han alterado.
g) ¿Qué significa que un aminoácido es anfótero?
Que un aminoácido sea anfótero quiere decir que puede actuar como ácido y como base, en función de las condiciones del medio. Esto permite la regulación del pH.
Cuando el medio es ácido, el aminoácido se comporta como base y el grupo carboxilo capta protones, mientras que si se encuentra en un medio básico se comporta como ácido y el grupo amino libera protones al medio.
Si el aminoácido está en un pH en el cual adopta una forma dipolar neutra, ese nivel de pH se denomina punto isoeléctrico, es el medio ideal.
Hasta la próxima.



fuente: blog de biología google
fuente: pinterest google
fuente: blog de biología google
fuente: blog de biología google